國立陽明交通大學生物科技學院
111學年度第二學期逕行修讀博士學位開始辦理申請
(111年12月8日公佈)
一、申請資格:
(一)學士班具下列條件之一者:
1.學業成績平均85分以上,具研究潛力者。
2.名次在該班學生前10%以內,具研究潛力者。
3.經系所評定為成績優異,具研究潛力者。
(二)碩士班學生,修業期間學業成績在該前二分之一以內,或有其他特殊情形(如發表論文)經系所評定為成績優異,並具有明顯之研究潛力。
二、報名日期:111年12月27日起至112年1月3日截止。
三、繳交文件:
(一)申請書
(二)助理教授以上推薦函兩份以上,其中一份需由指導教授、系主任或所長推薦。
(三)歷年成績單(含各學期名次證明)。
(四)成果摘要(至多A4紙5頁)。
(五) 研究計畫(至多A4紙5頁)。
※上述1-5項資料於報名時繳交至系辦,並註明報考所別,否則無法受理。
(六)口試當天繳交口試報告摘要。
四、逕行修讀博士錄取名額:
生物科技學系3名
分子醫學與生物工程研究所1名
生物科技學院產學博士班1名
生醫科學與工程博士學位學程1名
五、評分標準:
(一)審查佔50﹪
(二)口試佔50﹪(其中過去成果佔80﹪,未來研究佔20﹪)
六、口試時間:112年1月11日(三)
七、口試地點:博愛校區賢齊館3樓
112學年度陽明交通大學生物科技學院碩士班甄試入學備取通知
112學年度碩士班甄試入學備取生名單及報到注意事項
即日起至111年12月8日(四)下午3點前 (不含六、日、國定假日)完成報到手續
一、報到地點:新竹市博愛街75號賢齊館325室。
二、報到登記時需攜帶以下資料:大學成績單正本、畢業證書正本
※未報到者視同放棄,缺額將由備取生依序遞補登記報到。
如欲放棄請填寫回覆放棄聲明書或回覆信件告知。
生物科技學系甲組
501004備1
501021備2
501027備3
501001備4
501029備5
501009備6
501024備7
501011備8
生物科技學系乙組
502020備1
502014備2
502011備3
502012備4
502018備5
502008備6
502003備7
502004備8
生物科技學系丁組
504007備1
504009備2
分子醫學與生物工程研究所甲組
505004備1
505016備2
505031備3
分子醫學與生物工程研究所乙組
506007備1
506005備2
506003備3
506008備4
楊進木教授與鄒協成副教授研究團隊發表研究成果於International Journal of Molecular Sciences
連結網址:https://www.mdpi.com/1422-0067/23/23/14958
Abstract
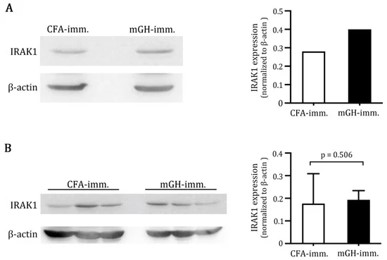
Autoimmune hypophysitis (AH) is an autoimmune disease of the pituitary for which the pathogenesis is incompletely known. AH is often treated with corticosteroids; however, steroids may lead to considerable side effects. Using a mouse model of AH (experimental autoimmune hypophysitis, EAH), we show that interleukin-1 receptor-associated kinase 1 (IRAK1) is upregulated in the pituitaries of mice that developed EAH. We identified rosoxacin as a specific inhibitor for IRAK1 and found it could treat EAH. Rosoxacin treatment at an early stage (day 0–13) slightly reduced disease severity, whereas treatment at a later stage (day 14–27) significantly suppressed EAH. Further investigation indicated rosoxacin reduced production of autoantigen-specific antibodies. Rosoxacin downregulated production of cytokines and chemokines that may dampen T cell differentiation or recruitment to the pituitary. Finally, rosoxacin downregulated class II major histocompatibility complex expression on antigen-presenting cells that may lead to impaired activation of autoantigen-specific T cells. These data suggest that IRAK1 may play a pathogenic role in AH and that rosoxacin may be an effective drug for AH and other inflammatory diseases involving IRAK1 dysregulation.
國立陽明交通大學112年度碩博士班甄試入學新生座談會暨備取生報到注意事項
1.請備取生請自行上生物科技學院公告查詢,不另通知。
2.本院謹訂於111年12月6日(二)上午10:00舉辦新生座談會並開放各實驗室參訪(中午備有餐點),非常歡迎備取生也參與當天座談會,一則可讓備取生提前瞭解可能遞補之機會,再則也可使將來遞補之備取生瞭解各位老師實驗室研究情形。
3.系(所)聯絡方式,電話:03-5729287、傳真:03-5729288
生物科技學院111學年新生座談會
時間:111年12月6日(星期二)
09:30–10:00正取生報到(地點:賢齊館310室)
10:00–10:30師生介紹(地點:賢齊館310室)
10:30–12:00參訪實驗室
12:00–13:00午餐(賢齊館310室)
13:00–16:00 參訪實驗室
碩博士班甄試榜單https://exam.nycu.edu.tw/action.aspx?id=09101c90-d6a0-4fbd-8804-7ac349a27d92
國立陽明交通大學112年度碩博士班甄試入學新生座談會暨正取生報到注意事項
1.請正取生親自攜身分證正本、歷年成績單、畢業證書正本,請於111年12月6日(星期二)上午九時三十分前,至博愛校區賢齊館310室辦理報到手續,逾時未報到者,以放棄錄取資格論。(報到時須繳驗學歷(力)證件,應屆畢業生尚未領取畢業證書者,可填寫切結書辦理報到。)另在職生須附上在職證明書正本。
2.本院謹訂於111年12月6日(二)上午10:00舉辦新生座談會並開放各實驗室參訪(中午備有餐點),歡迎正、備取生踴躍參加。
生物科技學院112學年新生座談會
時間:111年12月6日(星期二)
09:30–10:00正取生報到(地點:賢齊館310室)
10:00–10:30師生介紹(地點:賢齊館310室)
10:30–12:00參訪實驗室
12:00–13:00午餐(賢齊館310室)
13:00–16:00參訪實驗室
3.錄取系(所)聯絡方式,電話:03-5729287、傳真:03-5729288
4.切結書(附件1)
5.放棄聲明書(附件2)
碩博士班甄試榜單https://exam.nycu.edu.tw/action.aspx?id=09101c90-d6a0-4fbd-8804-7ac349a27d92
| 演講時間 | 111年11月22日 (星期二) 下午1:30至3:00 |
| 主講人 | 黃介辰教授 中興大學生命科學院院長 |
| 演講題目 | Back to the origin of life : from biological carbon fixation reactions to cell factory |
| 線上演說連結 | https://nycu.webex.com/nycu/j.php?MTID=m0f9171d79bade2d49b7d5294e17871d7密碼:0000 |
楊進木教授研究團隊發表研究成果於Front. Immunol.
連結網址:https://www.frontiersin.org/articles/10.3389/fimmu.2022.1080897/full
Abstract
Background: Drug repurposing is a fast and effective way to develop drugs for
an emerging disease such as COVID-19. The main challenges of effective drug
repurposing are the discoveries of the right therapeutic targets and the right
drugs for combating the disease.
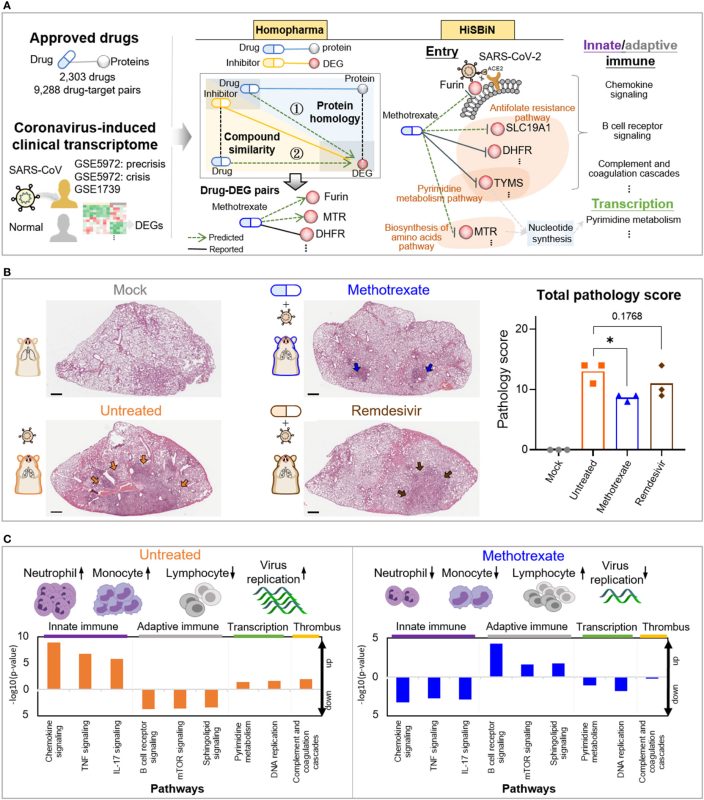
Methods: Here, we present a systematic repurposing approach, combining
Homopharma and hierarchal systems biology networks (HiSBiN), to predict 327
therapeutic targets and 21,233 drug-target interactions of 1,592 FDA drugs for
COVID-19. Among these multi-target drugs, eight candidates (along with
pimozide and valsartan) were tested and methotrexate was identified to
affect 14 therapeutic targets suppressing SARS-CoV-2 entry, viral replication, and COVID-19 pathologies. Through the use of in vitro (EC50 = 0.4 mM) and in
vivo models, we show that methotrexate is able to inhibit COVID-19 via
multiple mechanisms.
Results: Our in vitro studies illustrate that methotrexate can suppress SARSCoV-
2 entry and replication by targeting furin and DHFR of the host,
respectively. Additionally, methotrexate inhibits all four SARS-CoV-2 variants
of concern. In a Syrian hamster model for COVID-19, methotrexate reduced
virus replication, inflammation in the infected lungs. By analysis of
transcriptomic analysis of collected samples from hamster lung, we
uncovered that neutrophil infiltration and the pathways of innate immune
response, adaptive immune response and thrombosis are modulated in the
treated animals.
Conclusions: We demonstrate that this systematic repurposing approach is
potentially useful to identify pharmaceutical targets, multi-target drugs and
regulated pathways for a complex disease. Our findings indicate that
methotrexate is established as a promising drug against SARS-CoV-2 variants
and can be used to treat lung damage and inflammation in COVID-19,
warranting future evaluation in clinical trials.